| HOME情報公開推進局 認定基準 | |||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||
| 【基発第550号 昭和46年7月28日】 | |||||||||||||||||||||||||||||||||||||
| ○鉛、その合金又は化合物(四アルキル鉛を除く。)による疾病の認定基準について | |||||||||||||||||||||||||||||||||||||
| 標記の認定基準について、自今、下記のとおり改めることとしたので、その取扱いに遺憾のないようせられたい。 なお、本通達の施行に伴い、従来の標記認定基準に関する通達はこれを廃止する。 おって、個々の事案について、本通達の基準により難いか、もしくは判断が著しく困難な場合には、具体的資料を添えて本省にりん伺されたい。 |
|||||||||||||||||||||||||||||||||||||
記 |
|||||||||||||||||||||||||||||||||||||
| 鉛、その合金または化合物(四アルキル鉛を除く。)を取り扱い、あるいはそれらのガス、蒸気もしくは粉じんにさらされる業務に従事しているかまたはその業務に従事していた労働者が、次の各項の何れかに該当する場合には、労働基準法施行規則別表第1の2第4号の規定に基づく労働省告示第36号表中に掲げる鉛及びその化合物による疾病として取り扱うこと。 | |||||||||||||||||||||||||||||||||||||
| 1 | 次の各号に該当するものであること。ただし、(2)または(3)の何れかが基準値に満たない場合には、当分の間本省にりん伺すること。 | ||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||
| 2 | 次の各号に該当するものであること。 | ||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||
| 3 | 鉛の作用によることの明らかな伸筋麻ひが認められるものであること。 | ||||||||||||||||||||||||||||||||||||
上に戻る 解説 |
|||||||||||||||||||||||||||||||||||||
| 1 | 本通達(以下「新通達」という。)は、従来の通達(昭和25年6月27日付け基発第605号、昭和34年10月8日付け基発第693号、昭和39年9月8日付け基発第1049号)による鉛中毒に関する認定基準を改めたものである。すなわち、旧通達を策定した当時においては、いわゆる鉛中毒症等に関する診断方法、検査方法等が未だ開発途上にあったために、自他覚症状等当時まで慣用されてきた臨床手法にもとづいて認定基準を定めたものであるが、現在はこれらに関する診断並びに検査方法等が著しく進歩してきたので、それらの新しい検査方法等を加え、具体的事案の認定事務を公正、かつ、容易に行えるよう配慮し、改正したものである。 | ||||||||||||||||||||||||||||||||||||
| 2 |
|
||||||||||||||||||||||||||||||||||||
| 3 |
|
||||||||||||||||||||||||||||||||||||
| 4 | 新通達の記の1の(3)の血中または尿中の鉛量の測定については、原則として別紙(3)の検査方法によることとし、これにより検出された数値により判断すること。 | ||||||||||||||||||||||||||||||||||||
| 5 | 新通達の記の1及び2に示した検査の結果による数値は、いわゆる誘発法(Provocation test または Mobilization test)を行った後の測定値ではない。 なお、鉛中毒の診断に当り、症例によってはいわゆる誘発法が行われる場合があるが、これが取扱いについては、当面別紙(4)によること。 |
||||||||||||||||||||||||||||||||||||
| 6 | 新通達に示した尿中コプロポルフィリン、尿中デルタアミノレブリン酸、血中鉛、尿中鉛に関する数値は、一般的には、これらの数値を超えた場合に、鉛中毒を疑わしめるものとして例示した症状のうちの軽微なものが発現することもあると考えられているものであるが、鉛中毒症の早期発見、早期治療を期する上から今回、これらの数値を採用したものである。 しかしながら、貧血、尿中コプロポルフィリン、尿中デルタアミノレブリン酸は、他の原因によっても、新通達の数値を超える場合もあるので、とくに、新通達の記の2の適用に当っては、他の疾病との鑑別診断の結果を検討の上、認定するよう留意すること。 |
||||||||||||||||||||||||||||||||||||
上に戻る 別紙(1) 尿中のコプロポルフィリンの検査方法 |
|||||||||||||||||||||||||||||||||||||
| 1 | 原理 | ||||||||||||||||||||||||||||||||||||
| 尿中コプロポルフィリン及びコプロポルフィリノーゲンは酢酸を含むエーテル層に最初にうつし、水洗後ヨードで酸化して、コプロポルフィリンを塩酸で抽出した後、再びpH3.5としてこれをエーテル層にうつし、1N塩酸で抽出して吸光度を計測する。 |
|||||||||||||||||||||||||||||||||||||
| 2 | 器具と試薬 | ||||||||||||||||||||||||||||||||||||
| (1) | 器具 | ||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||
| (2) | 試薬 | ||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||
| 3 | 測定法 | ||||||||||||||||||||||||||||||||||||
| 分液ロート(約300ml) に新鮮尿を 25ml とり、これに氷酢酸 2.5ml を加える
(注1)。ついで精製エーテル 50ml を加え、30秒間よく振とうして放置する。水層を分離し、精製エーテル
25ml で再抽出する。次に蒸留水で2~3回軽く静かにエーテル層を洗う。水層を捨てる。あまり強く振ると、コプロポルフィリンが水層にうつるおそれがある。 残ったエーテル層に 0.005% ヨード液 5~10ml を加え、コプロポルフィリノーゲンをコプロポルフィリンに酸化する。 最後に 1N塩酸で、5ml、2ml、2mlずつ3回エーテル層のコプロポルフィリンを抽出し、目盛付共栓試験管にうつし、精製アルコールで 10ml とし、混和して 1cm の厚さのセルを用いて、光度計 380mμ、401mμ、430mμ の吸光度をしらべ、次式によって計算する。 { 2×OD401 - ( OD430 + OD380 ) } × 837 x v / V = μg ・ コプロポルフィリン / L ( V = 尿量、 v = 抽出塩酸量 ) |
|||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||
| 上に戻る |
|||||||||||||||||||||||||||||||||||||
| 別紙(2) 尿中デルタアミノレブリン酸測定法 |
|||||||||||||||||||||||||||||||||||||
| 1 | 原理 | ||||||||||||||||||||||||||||||||||||
| 浦田グラニック法 ( J.Biochem、 Vol 238. PP881. 1963 ) 2種類のイオン交換樹脂を用いて、δ‐ALAを分離し、ALAピロールをつくりこれをエールリッヒ試薬によって赤色に発色させ、比色定量する。 |
|||||||||||||||||||||||||||||||||||||
| 2 | 器具 | ||||||||||||||||||||||||||||||||||||
| カラム (3) 内径 9mm 前後 長さ 30cm 但し、3本のうち1本は長さ 10cmのものでよい。 比色計 (1) 552mμ フィルター式の場合はその近くのフィルターを用いる。 その他、試験管、pH メーター又は pH 試験紙、三角フラスコ、ガラス棒、ピペット類、煮沸用湯浴器、ロート、脱脂綿、純水。 ( ) 内は 1検体当りの本数 |
|||||||||||||||||||||||||||||||||||||
| 3 | 試薬 (後記「参考」参照) | ||||||||||||||||||||||||||||||||||||
| ○ 陽イオン交換樹脂 100~200 メッシュ ○ 陰イオン交換樹脂 (強塩基性) 200~400 メッシュ ○ メタノール(特) ○ 氷酢酸 ○ 酢酸ソーダ(特) アセチルアセトン ○ 塩酸 ○ 水酸化ナトリウム ○ 塩化第二水銀(特) ○ 過塩素酸(特) ○ パラジメチルアミノベンズアルデヒド(特) |
|||||||||||||||||||||||||||||||||||||
| 4 | 試薬の調製 | ||||||||||||||||||||||||||||||||||||
| (1) | 樹脂の調製 陽イオン交換樹脂について 1検体 7ml 程度必要 三角フラスコに必要量をとり、純水を10~20倍量加えて振る、放置、上清をすてる。 以上を上清が清澄になるまで (3~4回) くり返す。上清を捨て、1M・NaOH を樹脂の10倍量加えて混合、1晩放置。 上清を捨て、樹脂の10~20倍量の純水で10回ほど洗糠をくり返すと、pH がアルカリ性でなくなる。 1N・HCl で2回洗う。 HCl がなくなるまで、水で洗う。約10回 酢酸緩衝液 (pH4.8) を入れておく。 |
||||||||||||||||||||||||||||||||||||
| (2) | 樹脂の調製 陰イオン交換樹脂 (強塩基性) について 1検体 5ml 程度必要 (1) のように、水で洗い、ゴミなど除く。 3N、酢酸ソーダを樹脂の10倍量加え、これで3回洗う。もう1度これを加え、1晩放置 アルカリ性でなくなるまで水で洗う。 酢酸ソーダは特級のものでも、クロールイオン cl- を多量に含むものがあるので事前に硝酸銀でチェックするとよい。 以上の調製法は、バッチ法である。原法はカラムを用いているが、これだと時間がかかる。 |
||||||||||||||||||||||||||||||||||||
| (3) | 酢酸バッファー(pH4.6)1M 氷酢酸 57ml \ + 水を加えて1Lにする。 酢酸ソーダ 136g / pH4.8 の酢酸バッファーは、それぞれ、45ml と 100g を加え水で 1L にする。 |
||||||||||||||||||||||||||||||||||||
| (4) | エールリッヒ試薬 以下のものを、その都度つくる。5ml /検体必要 パラジメチルアミノベンズアルデヒド 4g 氷酢酸 168ml 過塩素酸 40ml 塩化第二水銀 0.7g 以上の混合物に、水を加えて全量 200ml とする。 |
||||||||||||||||||||||||||||||||||||
| (5) | メタノール酢酸混合物 容量で、2:1 に混合 |
||||||||||||||||||||||||||||||||||||
| (6) | 1M酢酸 | ||||||||||||||||||||||||||||||||||||
| 5 | 力ラムと尿の調製 | ||||||||||||||||||||||||||||||||||||
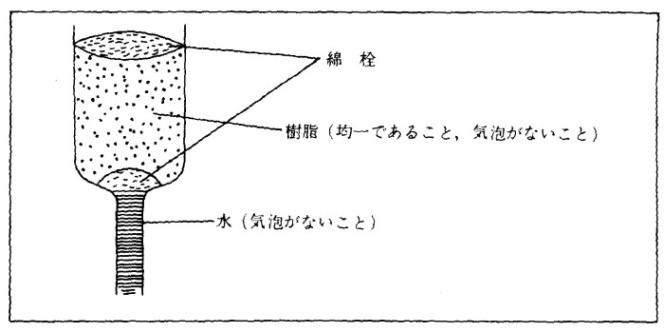
| (1) | カラムの調製 第1カラム 調製した陰イオン交換樹脂 第2カラム 〃 陽 〃 第3カラム 〃 陰 〃 1検体につき3本のカラムをスタンドに垂直にたて、綿栓をつめ、水を流す。 駒込ピペットで、上記樹脂を均一につめていく。 第1、2、3カラム、それぞれ 3、7、1cm の高さまでつめる。 つめたら、その上に綿栓をおく。(図) |
||||||||||||||||||||||||||||||||||||
 |
|||||||||||||||||||||||||||||||||||||
| (2) | 尿の調製 | ||||||||||||||||||||||||||||||||||||
| 普通の人の尿で 3.Oml 、鉛作業者では ALA の排泄量によるが、その 1/2~1/3 量を試験管にとり、pH を 5 % 酢酸で 5~6 に調節する。 | |||||||||||||||||||||||||||||||||||||
| 6 | 操作 | ||||||||||||||||||||||||||||||||||||
| (1) | 検体を完全に第1カラムに流し込む。流出液を下で試験管に受ける。 | ||||||||||||||||||||||||||||||||||||
| (2) | 流下終了後、純水 6ml を同一カラムに流し、(1)の試験管に受ける。 | ||||||||||||||||||||||||||||||||||||
| (3) | (1) と (2) とをあわせたもの (流出液) を第2カラムに流し込む。流出液を下で試験管 (20~30ml ) に受ける。 | ||||||||||||||||||||||||||||||||||||
| (4) | 流下終了後、純水 10ml をこのカラムに流し洗う。 洗液は一緒にする。 |
||||||||||||||||||||||||||||||||||||
| (5) | (4)の流出液に、酢酸バッファー 1ml とアセチルアセトン 0.5ml を加え、よく混合。 | ||||||||||||||||||||||||||||||||||||
| (6) | 沸騰水溶中に10分間浸し、煮沸する。 | ||||||||||||||||||||||||||||||||||||
| (7) | 放冷後、第3カラムに流す。流出液はすててよい。 ALAピロールはここに濃縮捕捉される。 |
||||||||||||||||||||||||||||||||||||
| (8) | 1M酢酸 5ml をこのカラムに流して洗う。流出液はすてる。 | ||||||||||||||||||||||||||||||||||||
| (9) | 10ml 目盛付試験管をカラムの下に置き、カラムにメタノール酢酸 4ml を流し、ALAピロールを流出せしめる。 | ||||||||||||||||||||||||||||||||||||
| (10) | 5ml の目盛までメタノール酢酸を加える。 | ||||||||||||||||||||||||||||||||||||
| (11) | エールリッヒ試薬 5.0ml を加え、混合。 | ||||||||||||||||||||||||||||||||||||
| (12) | 混合後15分で比色 552mμ | ||||||||||||||||||||||||||||||||||||
| 7 | 標準線の作成 | ||||||||||||||||||||||||||||||||||||
| 原法は、Molar absorbancy 5.3 × 10,000 として、計算している。 ALAは容易に手に入るので、これを購入して、自ら検量線を作ってもよい。その場合は次のようにする。 |
|||||||||||||||||||||||||||||||||||||
| (1) | ALA標品 | ||||||||||||||||||||||||||||||||||||
| ALA・HCl 分子量 167.6 ALA 分子量 131.1 (ALA塩酸塩結晶 100mg がアンプル入りで売り出されている。) |
|||||||||||||||||||||||||||||||||||||
| (2) | 適用量の ALA・HCl を化学天秤で正確に秤りとり、水を加え、pH を 5~6 に調節、更に水を加えて、ALA として、10mg/l の標準液をつくる。 | ||||||||||||||||||||||||||||||||||||
| (3) | これを稀釈して、1、2、3、5mg/l の濃度階段の標準液稀釈系列をつくって、尿と同様の操作で分離、比色する。 | ||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||
上に戻る 参考 |
|||||||||||||||||||||||||||||||||||||
| 試薬中の陽イオン交換樹脂及び陰イオン交換樹脂については、浦田グラニック法の場合、次のものが用いられている。 陽イオン交換樹脂 …… アンバーライト IRC50 陰 〃 …… ダウエックス 1 × 8 |
|||||||||||||||||||||||||||||||||||||
| 別紙(2) 別添 尿中デルタアミノレブリン酸測定法 |
|||||||||||||||||||||||||||||||||||||
| 原理 | |||||||||||||||||||||||||||||||||||||
| δ‐ALA はアセチルアセトンとの縮合によりピロールを作る。ピロールはエールリッヒ試薬のP-ジメチルアミノベンツアルデヒドと酸性溶液で赤色化合物を形成する。エールリッヒ試薬による反応に影響を及ぼす尿中の還元物質はあらかじめカラムにより分離を行う。 | |||||||||||||||||||||||||||||||||||||
| 試薬および器具(後記「参考」参照) | |||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||
定量操作法 |
|||||||||||||||||||||||||||||||||||||
| 1 | 前処理 | ||||||||||||||||||||||||||||||||||||
| 陰イオン交換樹脂は水洗後 3M の酢酸ソーダ溶液でクロライドフリーになるまで洗い、次に酢酸ソーダがフリーになるまで蒸留水で洗涙する。 陽イオン交換樹脂は水洗後 2N-苛性ソーダで一夜放置し、蒸留水で中性になるまで洗涙する。 |
|||||||||||||||||||||||||||||||||||||
| 2 | 定量操作 | ||||||||||||||||||||||||||||||||||||
| 第1カラム (内径 10mm)、第2カラム (内径 8mm)のそれぞれの底部に樹脂の流出を防ぐためグラスウールを
2~3mm つめる。 第1カラムには蒸留水に浮かした陰イオン交換樹脂を駒込ピペットで 3ml 入れる。 第2カラムには陽イオン交換樹脂を同様に入れ、1.5cm くらいの高さとする。それぞれ蒸留水を通す。流速は 3ml / 10min とする。第2カラムには 4N-塩酸 1ml 1回、2N-塩酸 5ml 1回、1N-塩酸 5ml 1回を通す。蒸留水で中性になるまで洗涙する。 |
|||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||
| 3 | 力ラムの再生 | ||||||||||||||||||||||||||||||||||||
| 第1カラムは1M-酢酸 2ml、0.2M-酢酸 2ml で2回洗い、蒸留水で中性になるまで洗糠する。 第2カラムは蒸留水で中性になるまで洗涙する。 |
|||||||||||||||||||||||||||||||||||||
| 試算 | |||||||||||||||||||||||||||||||||||||
| 吸光度 x 47 = mg/l | |||||||||||||||||||||||||||||||||||||
| 参考 | |||||||||||||||||||||||||||||||||||||
| 試薬中の陰イオン交換樹脂及び陽イオン交換樹脂については、Mauzerall-Granick
法の場合次のものが用いられている。 陰イオン交換樹脂 …… ダウエックス 2 x 8 陽 〃 …… ダウエックス50× 8 |
|||||||||||||||||||||||||||||||||||||
上に戻る |
|||||||||||||||||||||||||||||||||||||
| 別紙(3) 血中及び尿中の鉛の検査方法 |
|||||||||||||||||||||||||||||||||||||
| 1 | 目的と原理 | ||||||||||||||||||||||||||||||||||||
| 鉛業務従事作業者にみられる血中及び尿中の鉛量の増加の程度を測定することにより、鉛への暴露の程度ないしは鉛中毒罹患の有無を判定する資料とする。 ジチゾン (diphenylthiocarbazone: Dz と略す。) 液はクエン酸を含む pH9~12 の弱アルカリ溶液中で鉛イオンと錯塩を作り、有機溶媒に抽出されて特有の呈色を示す。これを比色定量とする。 |
|||||||||||||||||||||||||||||||||||||
| 2 | 器具と試薬 | ||||||||||||||||||||||||||||||||||||
| (1) | 器具 | ||||||||||||||||||||||||||||||||||||
| イ 採血用具一式 ロ 注射筒 (20ml) ハ 注射針 (1/1) 二 採尿容器(ポリエチレン広口 1,000ml以上) ホ 石英容器(ビーカー 200ml 以上):乾式灰化用 へ 電気炉 ト ケルダールフラスコ (200ml以上):湿式灰化用 チ ろ過器 (石綿又はガラス) リ 電熱板又は赤外線ランプ ヌ 分液ロート (100~300ml 数回及び 1L ) ル 目盛付共栓付試験管 (20ml ):検定済 ヲ 分光光度計又は 510~520mμのフィルターを有する光電比色計 ワ 乳鉢、ろ紙、水浴、蒸留器 塩ビ製品は鉛の溶出が多いのでつかわないこと。 <器具の清浄法> 注射筒及び鉛を含まないガラス、及び石英の器具は最初クロム硫酸に浸漬したのち、水洗し、次いで 5 % 硝酸で約10分間煮沸したのち精水で十分洗浄し、乾燥して使用する。注射針は 1 % 硝酸、次いで精水をよく通して洗い、精水で10分間煮沸乾燥する。採尿容器は 30 % 硝酸であらかじめよく除鉛しておき、精水で洗浄乾燥させる。 なお、塩ビ製品は鉛の溶出が多いので用いない。 |
|||||||||||||||||||||||||||||||||||||
| (2) | 試薬 | ||||||||||||||||||||||||||||||||||||
| 除鉛操作をするものでもなるべく試薬特級を用いる。クロロホルムは試薬1級を精製する。ジチゾン試薬特級(重金属鉛として 0.002 % 以下)を使用する。 | |||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||
| 3 | 検量曲線 | ||||||||||||||||||||||||||||||||||||
| 鉛標準液を1%硝酸で、それぞれ 1~50μg の鉛を含む溶液 50ml ずつを各濃度ごとに作り、これを分液ロートにとり、Dzクロロホルム溶液
10ml、シアン化カリウム、アンモニア水混合液 10ml を加えて直ちに強く振とうする。分層したクロロホルム層を比色計にかけて吸光度を知り検量曲線を作製する。 一例を示すと次のごとくである。
|
|||||||||||||||||||||||||||||||||||||
| 4 | 試薬の採取 | ||||||||||||||||||||||||||||||||||||
| (1) | 血液採取する血液量は10~20g とする。 | ||||||||||||||||||||||||||||||||||||
| (2) | 尿なるべく24時間尿から約100ml を定量用に供する。作業場で蓄尿するときには外部からの汚染をさけるように注意すること。 | ||||||||||||||||||||||||||||||||||||
| 5 | 試料の前処理 | ||||||||||||||||||||||||||||||||||||
| (1) | 乾式灰化法 | ||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||
| (2) | 湿式灰化法 | ||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||
| 6 | 測定 | ||||||||||||||||||||||||||||||||||||
| (1) | ジチゾン単色法 | ||||||||||||||||||||||||||||||||||||
四塩化炭素を用いる方法もあるが、より簡便な方法としてベンゼン法(尿中鉛測定簡便法)をとりあげた。
|
|||||||||||||||||||||||||||||||||||||
| (2) | ジチゾン混色法 | ||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||
上に戻る |
|||||||||||||||||||||||||||||||||||||
| 附1 ポーラログラフ法 |
|||||||||||||||||||||||||||||||||||||
| イ | Dz混色法と同様にして得た酸性試料溶液に、チモールブルー数滴とクエン酸アンモニウム液 5~10ml 加え、アンモニア水で pH8.5~9.0 とする(この際白色沈澱物を生じたならばさらにクエン酸アンモニウム液を追加することにより溶解せしめうる。)。 | ||||||||||||||||||||||||||||||||||||
| ロ | この試料液を分液ロート (a) に移し、原容器に水で数回内部を洗って (a) を加える。次に塩酸ヒドロキシルアミン液 1ml を加え、アンモニア水で pH8.5~9.0 調整し、さらに 10 % シアン化カリウム 5ml を加え混合する。その後これにDz液 1ml を加え強く振とうする。静置により分層したDz層の色を記憶しておく (後で1N塩酸を加えるときの参考とする。)。 さらにDz液 2ml を加え、強く振とう静置後Dz層を第2の分液ロート (b) に分別する。加えたDz液が振とう後も原色のままで残るまで (a) の振とう分別をくり返し、Dz層を (b) に加える。 |
||||||||||||||||||||||||||||||||||||
| ハ | (b) に最初呈したDz層の色に応じて、1N-塩酸を加える (Dz層が緑ないし帯緑紫のときは 3ml、エンジないし朱紅のときは 5ml 程度をメスピペットで、正確に加える。)。強く振とうすることにより鉛はDzから離れて塩酸層に移行し、Dz層は原色たる緑色にかえる。しばらく放置した後Dz層は捨てる。 | ||||||||||||||||||||||||||||||||||||
| ニ | ポーラロ用セルに分液ロートの上部より塩酸層を約 2ml 入れる。次にセルに水銀少量を入れ10~15分間窒素ガスを導入し、酸素を追い出す。 | ||||||||||||||||||||||||||||||||||||
| ホ | (-) 0.35V ~ (-) 0.6V VS.S.CE の間で型のとおりにポーラログラフ操作を行う。ここに1N-塩酸では鉛の半波電位は(-) 4.3V VS.S.CEである。 | ||||||||||||||||||||||||||||||||||||
上に戻る 原子吸光分析法による尿中および血中鉛量の測定法 |
|||||||||||||||||||||||||||||||||||||
| 原理 | |||||||||||||||||||||||||||||||||||||
| 原子吸光分析は、原子が活性化される時に光を吸収する現象を利用した分析法である。金属元素は炎の中で熱解離して原子状態になるが、この状態が最も安定した電子配列を有する基底状態である。基底状態の原子にほかからのエネルギーを加えると、このエネルギーを吸収して励起状態になる。従って原子蒸気を一定の温度で熱平衡を保たせておくと、一部は励起状態、他の一部は基底状態となる。特定の金属元素を炎に入れて原子蒸気とし、ほかから同じ元素のスペクトルを出す連続光を当てると、透過する連続光は吸収されて暗くななる。この吸収を利用したものが原子吸光(吸収)法である。 | |||||||||||||||||||||||||||||||||||||
| Ⅰ 尿中および血中鉛量のジチゾン抽出、原子吸光測定法 | |||||||||||||||||||||||||||||||||||||
| 1 | 試薬 | ||||||||||||||||||||||||||||||||||||
| 1) | 硝酸 | ||||||||||||||||||||||||||||||||||||
| 2) | 硫酸 | ||||||||||||||||||||||||||||||||||||
| 3) | 過塩素酸 | ||||||||||||||||||||||||||||||||||||
| 4) | クエン酸アンモニア溶液 クエン酸 50g を水に溶かし、アンモニアでアルカリ性とし (pH約9.5)、水を加えて全量を 100ml とする、適当な濃度のジチゾンクロロホルムで鉛を除去したのち使用する。 |
||||||||||||||||||||||||||||||||||||
| 5) | 指示薬チモールブルー溶液 チモールブルーを少量のエチルアルコールに溶かし、さらに水を加えて溶液とする。溶液は 0.04 % 位でよい。 |
||||||||||||||||||||||||||||||||||||
| 6) | アンモニア水 | ||||||||||||||||||||||||||||||||||||
| 7) | 5 % シアン化カリウム液 水 100ml にシアン化カリウム 5g を溶かして作る。適当な濃度のジチゾンクロロホルムで鉛を除去したのち使用する。 |
||||||||||||||||||||||||||||||||||||
| 8) | 20 % 塩酸ヒドロキシルアミン溶液 塩酸ヒドロキシルアミン 20g を水に溶かし、アンモニア水でアルカリ性とし、さらに水を加えて全量を 100ml とする、適当な濃度のジチゾンクロロホルムで鉛を除去したのち使用する。 |
||||||||||||||||||||||||||||||||||||
| 9) | ジチゾンクロロホルム ジチゾンクロロホルムは、分液ロート中でジチゾン 100mg をクロロホルムに溶かし水洗後、水を加え、アンモニア水でアルカリ性にして振る。ジチゾンは水層に移る。水層をクロロホルムで洗浄し、クロロホルム層が淡緑色になるまでくり返す。水層を残し、水層を塩酸で酸性にし、クロロホルムを加えて振ると、ジチゾンはクロロホルムに移る。これを水洗して塩酸を除去して使用する。 |
||||||||||||||||||||||||||||||||||||
| 10) | 0.5 % シアン化カリウム溶液 シアン化カリウム 0.5g を水 100ml に溶かして作る。適当な濃度のジチゾンクロロホルムで鉛を除去しておく。 |
||||||||||||||||||||||||||||||||||||
| 11) | 2 % 硝酸 硝酸 2ml をとり、水で 100ml とする。 |
||||||||||||||||||||||||||||||||||||
| 12) | 鉛基準液 硝酸鉛 1.60g を精秤し、水に溶かし、硝酸 (1 + 1 ) 1ml を加えメスフラスコ 1L に入れ、水で全量を 1L とする。この溶液 1ml を正しくメスフラスコ 1L にとり、2 % 硝酸で標線までうすめる。この溶液は 1ppm 溶液である。 同様にして各種 ppmの鉛硝酸溶液を作成する。 |
||||||||||||||||||||||||||||||||||||
| 注意事項 | |||||||||||||||||||||||||||||||||||||
| (1) | 硝酸、硫酸、過塩素酸の鉛を除去することは大変である。従って出来るだけ鉛の少ないものを使用しなければならない。鉛定量用のものでもかなり鉛を含んでいることがあるから注意すること。 | ||||||||||||||||||||||||||||||||||||
| (2) | 試薬はすべて特級を使用すること。 | ||||||||||||||||||||||||||||||||||||
| (3) | 鉛基準液は原子吸光測定のさい2%硝酸を用いるので、2 % 硝酸溶液としておく。 | ||||||||||||||||||||||||||||||||||||
| (4) | 市販のジチゾンは、すでに酸化されているものを含んでいる場合もあるので、それを確認し、必要ならば純化しなければならない。 | ||||||||||||||||||||||||||||||||||||
| 2 | 器具 | ||||||||||||||||||||||||||||||||||||
| 1) ケルダールフラスコ 2) 分液ロート 3) 試験管(共栓試験管を含む。) 4) ピペット類、メスシリンダー、ビーカーなど一式 5) 湿式灰化のための熱源装置一式 6) 原子吸光分光光度計一式 |
|||||||||||||||||||||||||||||||||||||
| 注意事項 | |||||||||||||||||||||||||||||||||||||
| (1) | ケルダールフラスコ、分液ロート、試験管、ビーカーなどは超硬質ガラス(無鉛ガラス)製のものを使用すること。 | ||||||||||||||||||||||||||||||||||||
| (2) | ガラス器具類はすべて10 % 硝酸に浸しておき、よく水洗したのち純水または鉛のない蒸留水で再水洗したのち使用する。 | ||||||||||||||||||||||||||||||||||||
| 3 | 操作 | ||||||||||||||||||||||||||||||||||||
| 1) | 灰化
|
||||||||||||||||||||||||||||||||||||
| 2) | 灰化液を純水または鉛のない蒸留水約 50ml を用いて分液ロートヘ移す。 | ||||||||||||||||||||||||||||||||||||
| 3) | 次いでクエン酸アンモニア溶液 5ml を加える。 | ||||||||||||||||||||||||||||||||||||
| 4) | 指示薬チモールブルー溶液5~6滴加える。 | ||||||||||||||||||||||||||||||||||||
| 5) | アンモニア水でアルカリ性とする。鉛はpH8.5~11 で抽出できるが、pH9.0~9.5 位がよい。 | ||||||||||||||||||||||||||||||||||||
| 6) | 5 % シアン化カリウム溶液 5ml を加える。 | ||||||||||||||||||||||||||||||||||||
| 7) | 20 % 塩酸ヒドロキシルアミン溶液 1ml を加える。 | ||||||||||||||||||||||||||||||||||||
| 8) | 5ml のジチゾンクロロホルムで2回抽出し、クロロホルムを試験管に合せておく。これで抽出が完了しない場合にはさらにこの操作をくり返す。抽出が終ればクロロホルムは緑色のままである(シアン化カリウムによっては緑色を消すことがあるので注意を要する。)。抽出が終ってからジチゾンの入っていないクロロホルムを少量加えて振り、クロロホルムをさきの試験管に合せておく。 | ||||||||||||||||||||||||||||||||||||
| 9) | 試験管に集めたクロロホルムを分液ロートに移し、0.5 % シアン化カリウム溶液 20~30ml で軽く洗い、さらに20~30ml の水で軽く洗ってから、共栓付試験管に移し、2 % 硝酸 100ml を加えて強く振る。このさい水層がクロロホルム層に入り込んでいると、水層はアルカリ性があるため、2 % 硝酸の酸度が落ち、鉛の硝酸への移行が悪くなる。従って水層が少しでもクロロホルム層に入らないように注意しなければならない。 | ||||||||||||||||||||||||||||||||||||
| 10) | 硝酸層の鉛濃度を原子吸光分光光度計によって測定する。共栓試験管を用いるさいにはその上層の硝酸層をそのまま噴霧して測定できる。 | ||||||||||||||||||||||||||||||||||||
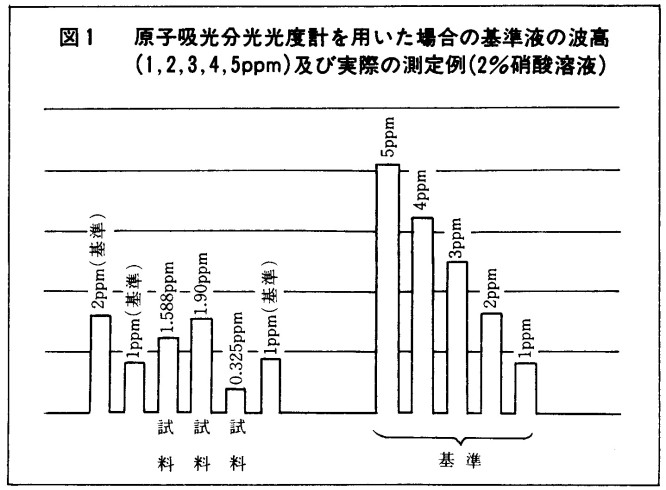
| 11) | 基準としては 1ppm (時には 2ppm、3ppm など)のものを噴霧測定して、その波高を基準とする。 1ppm、2ppm、3ppm などの基準液で検量線を作成してもよい (図1)。 |
||||||||||||||||||||||||||||||||||||
 |
|||||||||||||||||||||||||||||||||||||
| 注意事項 | |||||||||||||||||||||||||||||||||||||
| (1) | 本方法では尿中鉛量 10μg/L、血中鉛量10μg/100g 程度から測定可能である(実際には 5μg 程度から測定できる。)。尿の場合で本方法により測定できない場合には尿量を増やして測定し直すか、硝酸層を濃縮して測定すればよい。血液の場合も同様硝酸層を濃縮して測定することも可能であるが、鉛量が非常に少いことが予測され、この方法で測定不可能と考える場合(ジチゾン抽出の際にでも分るが)には、逆抽出の 2 % 硝酸を 5ml にすればよい。 | ||||||||||||||||||||||||||||||||||||
| (2) | 本方法でジチゾン抽出をすれば、カドミウムは masking できないので (カドミウムは masking する方法はない。)、原子吸光測定する硝酸層には鉛とカドミウムが共存することになる。すなわちカドミウムと鉛を同時抽出することが可能であるということでもある。しかしカドミウムイオンは、鉛イオンによって干渉され、測定値が高くなるので、カドミウムを測定する場合には別に抽出のさいの pH を 12以上 (pH13.5 位の方がよい。)にして、鉛をジチゾンとキレートさせずに単独に抽出した方がよい。反対に鉛のジチゾンによる単独抽出は不可能である。比色の場合にはジチゾン鉛も、ジチゾンカドミウムも最大吸収波長 520mμ 前後の赤(ピンク)色を呈するので、混合されて比色されていることになる。原子吸光測定の場合には鉛イオンは、尿中カドミウム量として 10μg/L、血中カドミウム量として 10μg/100g 程度までのカドミウムイオンによっては干渉されないので、通常の場合にはカドミウムイオンの存在は考慮に入れなくてよい。従って原子吸光測定の方が比色法より正確な値を得ることができる。 | ||||||||||||||||||||||||||||||||||||
| (3) | 本方法はジチゾンクロロホルムを使用する混色法を採用した。ジチゾン抽出には四塩化炭素、ベンゼンを用いる単色法もあり、夫々長所をもっているが、数多くの検体をとり扱う場合の検査員の中毒の危険性を考えてクロロホルムを採用した。 | ||||||||||||||||||||||||||||||||||||
| (4) | 本方法で最も重要なポイントはジチゾン抽出を完全にすること、硝酸へ移すさいに硝酸層へ水層を入れないことである。特に後者に注意すべきである。 | ||||||||||||||||||||||||||||||||||||
| (5) | 希硝酸で逆抽出せずにクロロホルムや四塩化炭素、ベンゼンのまま測定する方法も考えられるが、クロロホルムや四塩化炭素はフレームが不安定であり、ベンゼンはフレームが非常に大きく白熱し、ススが出る(武内ら5)ので測定は感心しない。従ってジチゾン抽出のさいは、どの方法をとっても希硝酸に逆抽出して測定しなければならない。 | ||||||||||||||||||||||||||||||||||||
| (6) | 測定にさいしてはその都度盲検値を測定しておかねばならない。また試薬の全ブランクは 1μg 以下であることが望ましく、そのようにすることは可能である。 | ||||||||||||||||||||||||||||||||||||
| (7) | 原子吸光測定は僅かであるが経時変化する。またホロー・カツード、ランプは使用時間によって感度が低下して来る。従って基準はできるだけ頻繁に測定しておく必要がある。デジタル表示の原子吸光分光光度計を使用するさいにも経時変化とランプの感度低下に気をつけて対処しなければならない。また、検量線を使用する場合も、これらの点から再三、再四検量線を作成しなければならない。 | ||||||||||||||||||||||||||||||||||||
上に戻る Ⅱ 尿中および血中鉛量のAPDC-MIBK抽出、原子吸光測定法 |
|||||||||||||||||||||||||||||||||||||
| A 尿中鉛の測定法〔灰化して測定する方法〕 | |||||||||||||||||||||||||||||||||||||
| 1 | 試薬 | ||||||||||||||||||||||||||||||||||||
| 1) | 硝酸 | ||||||||||||||||||||||||||||||||||||
| 2) | 硫酸 | ||||||||||||||||||||||||||||||||||||
| 3) | アンモニア水 | ||||||||||||||||||||||||||||||||||||
| 4) | 1 % ピロリジン、ジチオカルバミン酸アンモニウム(APDC)溶液 APDC 1g を水100ml に溶かして作成する。要すればろ過する。 | ||||||||||||||||||||||||||||||||||||
| 5) | メチルイソブチルケトン(MIBK) 水を飽和させる。 |
||||||||||||||||||||||||||||||||||||
| 6) | 鉛基準液 硝酸鉛 1.60g を精秤して水に溶かし、硝酸 (1 + 1) 1ml を加え、メスフラスコ1Lに入れ水で全量を 1L とする。この溶液 1ml を正しくメスフラスコ 1L にとり、水で殆んど標線までうすめ硝酸でpH を3.5 注1) に合せてから、さらに水を標線まで加える。この溶液 1ml は鉛 0.001mg を含む (1ppm 溶液)。 |
||||||||||||||||||||||||||||||||||||
| 2 | 器具 | ||||||||||||||||||||||||||||||||||||
| 1) ケルダールフラスコ 2) 分液ロート 3) 試験管 4) ピペット類、メスシリンダー、ビーカーなど一式 5) 共栓付遠沈管 (約50ml) 6) pH メーター 7) 遠心沈澱器 8) 湿式灰化のための熱源装置一式 9) 原子吸光分光光度計一式 10) 振盪機(できれば) |
|||||||||||||||||||||||||||||||||||||
| 注意事項 | |||||||||||||||||||||||||||||||||||||
| ケルダールフラスコ、分液ロート、試験管、遠沈管などは超硬質ガラス(無鉛ガラス)製を使用すること。ガラス器具はすべて10%硝酸に浸しておき、よく水洗したのち、純水または鉛のない蒸留水で再水洗して使用する。 | |||||||||||||||||||||||||||||||||||||
| 3 | 操作 | ||||||||||||||||||||||||||||||||||||
| 1) | 灰化 尿 50ml をケルダールフラスコにとり、硝酸、過塩素酸で湿式灰化をする。灰化法はジチゾン抽出原子吸光測定の場合の灰化(Ⅰ、3、1)、(イ)参照)と同様に行う。 |
||||||||||||||||||||||||||||||||||||
| 2) | 灰化液を純水または鉛のない蒸留水約 50ml で分液ロートに移し、アンモニア水でpH を3.5 注1)にする。 | ||||||||||||||||||||||||||||||||||||
| 3) | 次いで 1 % ピロリジン、ジチオカルバミン酸アンモニウム (APDC) 溶液 3ml を加え数分振り、さらにメチルイソブチルケトン (MIBK) 10ml を加えて数分振る。 | ||||||||||||||||||||||||||||||||||||
| 4) | 次に数分静置したのち共栓付遠沈管にMIBK層全部と水層の一部(入るだけ)を入れて遠沈したのち、MIBK層を噴霧測定する。 (注)出来るだけ早く測定すること。 | ||||||||||||||||||||||||||||||||||||
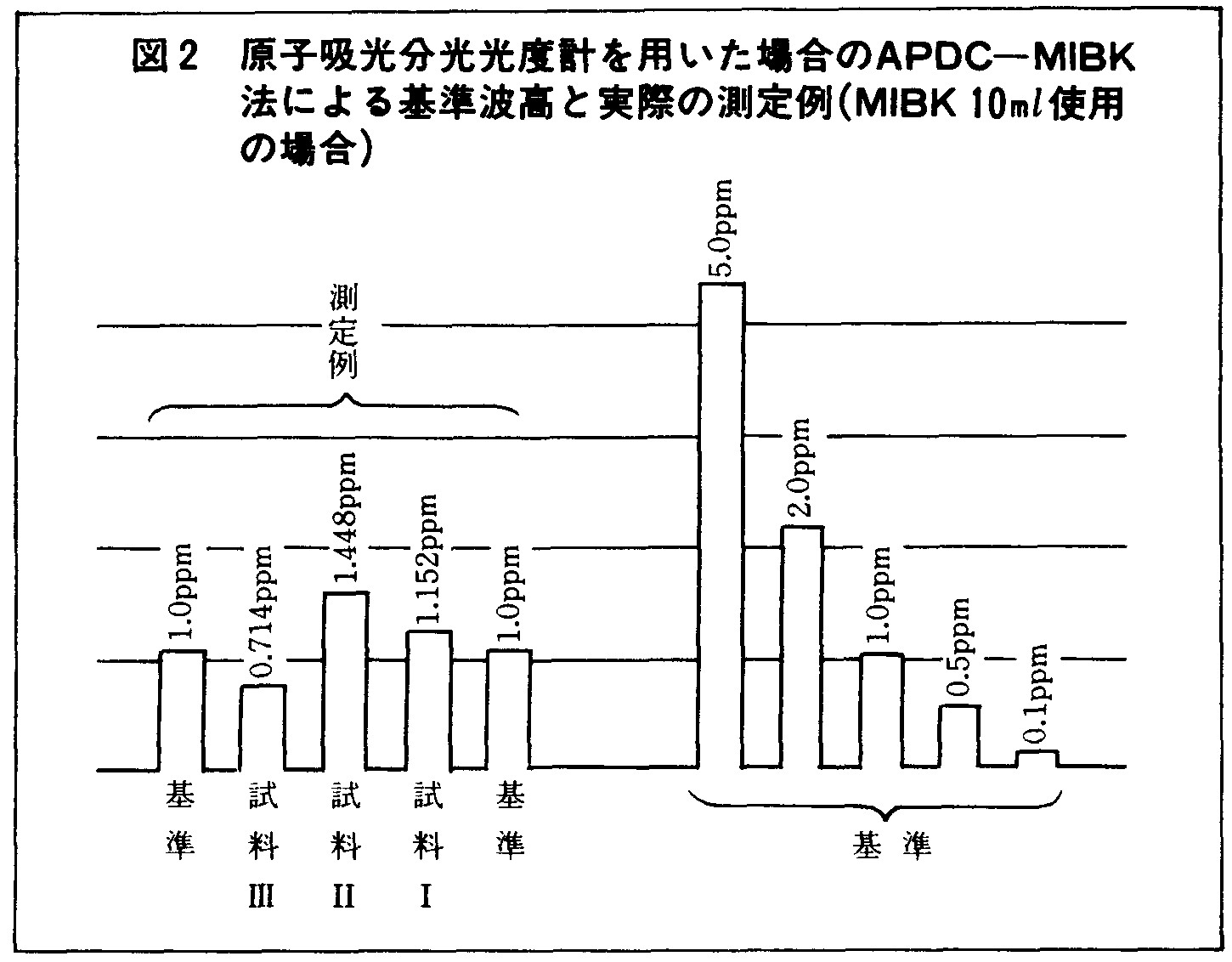
| 5) | 鉛基準液 (1ppm)、10ml (pH3.5) を共栓付遠沈管に入れ、1 % APDC 3ml、MIBK 10ml を加え強く振り、水層とMIBK層が分離してから、MIBK層を噴霧測定したものが 1ppmの基準波高である。この波高と試料の波高とを比べて鉛量を算定する (図2)。 | ||||||||||||||||||||||||||||||||||||
 |
|||||||||||||||||||||||||||||||||||||
| 検量線を作成して算出する場合には鉛基準液 5ml (0.5ppm)、10ml (1ppm)、15ml (1.5ppm)、20ml (2ppm) を同様共栓付遠沈管に入れ、夫々に 1 % APDC 3ml、MIBK 10ml を加えて振り、MIBK層を噴霧測定し、作成する。 | |||||||||||||||||||||||||||||||||||||
| 注意事項 | |||||||||||||||||||||||||||||||||||||
| (1) | 本方法で尿 50ml 使用する場合には尿中鉛量 4μg/L 程度のものから測定可能である。 | ||||||||||||||||||||||||||||||||||||
| (2) | この方法においても盲検値は必ず測定しておかねばならない。 | ||||||||||||||||||||||||||||||||||||
| (3) | 試薬ブランクはできるだけ少なくしておく必要がある。 | ||||||||||||||||||||||||||||||||||||
上に戻る B 血中鉛量の測定法〔灰化して測定する方法〕 |
|||||||||||||||||||||||||||||||||||||
| 1 | 試薬 | ||||||||||||||||||||||||||||||||||||
| 1) 硝酸 2) 硫酸 3) 過塩素酸 4) アンモニア水 5) 1 % ピロリジン、ジチオカルバミン酸アンモニウム (APDC) 溶液 尿中鉛の灰化して測定する方法の項(Ⅱ、A、1、4) )参照 6) メチルイソブチルケトン(MIBK) 尿中鉛の灰化して測定する方法の項(Ⅱ、A、1、5) )参照 7) 鉛基準液 尿中鉛の灰化して測定する方法の項(Ⅱ、A、1、6) )と同じ。 |
|||||||||||||||||||||||||||||||||||||
| 2 | 器具 | ||||||||||||||||||||||||||||||||||||
| 1) ケルダールフラスコ 2) 分液ロート 3) 試験管、ピペット類、メスシリンダー、ビーカーなど一式 4) 共栓付遠沈管(約 50ml ) 5) pHメーター 6) 遠心沈澱器 7) 湿式灰化のための熱源装置一式 8) 原子吸光分光光度計一式 9) 振盪機(できれば) |
|||||||||||||||||||||||||||||||||||||
| 注意事項 | |||||||||||||||||||||||||||||||||||||
| ケルダールフラスコ、分液ロート、試験管、遠沈管などのガラスの質、洗浄のさいの注意は、ジチゾン抽出原子吸光測定の項(Ⅰ、2の注意事項)参照。 | |||||||||||||||||||||||||||||||||||||
| 3 | 操作 | ||||||||||||||||||||||||||||||||||||
| 1) | 灰化 血液 5~10ml (10ml 使用の方がよい。)とり、予め秤量しておいたケルダールフラスコに入れ、再秤量して血液の重量を測定しておく。次いで硝酸、硫酸、過塩素酸の順に湿式灰化する。灰化はジチゾン抽出原子吸光測定の項(Ⅰ、3、1)、ロ) )の通りに行えばよい。 |
||||||||||||||||||||||||||||||||||||
| 2) | 灰化液を純水または鉛のない蒸留水約50mlで分液ロートに移し、アンモニア水でpHを3.5 に合せる。 | ||||||||||||||||||||||||||||||||||||
| 3) | 1 % APDC 25ml を加えて数分振り、次いで MIBK 10ml を加え数分振り、数分静置後、MIBK層と水層とが分離すれば、共栓遠沈管にMIBK層全部と入るだけの水量を入れて遠沈する。 | ||||||||||||||||||||||||||||||||||||
| 4) | 遠沈後MIBK層をできるだけ早く噴霧測定する。 | ||||||||||||||||||||||||||||||||||||
| 5) | 本方法では、血液中の鉄の存在が問題となるが 1 % APDC 25ml を用いれば、影響が少ない。ただし、アルカリ性でトリエタノールアミンで鉄をいんぺいする方法もあるが、この場合は、ジチオカルバミン酸ソーダを用いる。 | ||||||||||||||||||||||||||||||||||||
| 6) | 鉛の基準は尿中鉛の灰化して測定する方法の項(Ⅱ、A、1、6) )と同じようにする。 | ||||||||||||||||||||||||||||||||||||
| 注意事項 | |||||||||||||||||||||||||||||||||||||
| (1) | 本方法では血液 10ml 使用した場合には、血中鉛量 2μg/100g 程度のものから測定できる。 | ||||||||||||||||||||||||||||||||||||
| (2) | 測定にさいしてはその都度盲検値を測定しておくことが絶対必要である。 | ||||||||||||||||||||||||||||||||||||
| (3) | 試薬ブランクはできるだけ少なくすることが必要である。 | ||||||||||||||||||||||||||||||||||||
| (4) | 基準は頻繁に測定しておかねばならない。検量線を使用する場合にも検量線を頻繁に作成しなければならない。またデジタル表示の器械を使用される場合には注意が必要である。 | ||||||||||||||||||||||||||||||||||||
上に戻る |
|||||||||||||||||||||||||||||||||||||
| 別紙(4) CaNa2 EDTA等キレート剤の使用による尿中鉛量の測定に関する認定上の取扱いについて | |||||||||||||||||||||||||||||||||||||
| 1 | CaNa2 EDTA等キレート剤の使用による尿中鉛量の測定について | ||||||||||||||||||||||||||||||||||||
| (1) | 鉛中毒の診断に当たり、症例によっては、CaNa2 EDTA等キレート剤を使用した後の尿中鉛量の測定(以下「いわゆる誘発法」という。)を行って、当該労働者の従前の鉛暴露の状態を確認あるいは推定し、その影響を検討するための参考に資することがある。 もともと、CaNa2 EDTAは、鉛その他の重金属中毒の場合に、体内の重金属を置換して体外に排出することによって、当該中毒を治療するために用いられるものである。時によると副作用として、ショック、一過性の高血圧、腎障害、発疹等をひき起すおそれもあるので、いわゆる健康診断等の一方法として集団的に行うことは避け、個々の症例について問題のある次のような場合であって医師が必要と認めたときに、充分に事前の諸検査(とくに腎機能の検査)をつくして行われるものである 。 <症例> 現在は、鉛業務に従事していないが、過去に鉛業務に従事し、鉛暴露をうけたことのある労働者が、鉛中毒を強く疑わしめる症状を呈しているに拘らず、尿中コプロポルフィリン、尿中デルタアミノレブリン酸、血中鉛、尿中鉛の検査ではさしたる所見は認められない場合。 |
||||||||||||||||||||||||||||||||||||
| (2) | いわゆる誘発法は、普通は CaNa2 EDTAの20mg/kg (体重 1kg 当り 20mg )を
5 % ブドウ糖 250ml~500ml にとかし、1時間以上かけて徐々に点滴静脈注射して、注射開始から24時間の全尿を採尿し尿中鉛量を測定する方法が行われている。 なお、CaNa2 EDTA錠の使用は、結果の画一性が期待できないところから原則として避けるべきものとされている。 |
||||||||||||||||||||||||||||||||||||
| 2 | いわゆる誘発法による場合の認定上の取扱いについて | ||||||||||||||||||||||||||||||||||||
| いわゆる誘発法による結果、CaNa2 EDTAを注射開始から24時間の全尿について、500マイクログラム以上の鉛が検出され、かつ、次に該当する場合には、労働基準法施行規則別表第1の2第4号の規定に基づく労働省告示第36号表中に掲げる鉛及びその化合物による疾病として取扱うこと。 前記1の(1)の〔症例〕に該当する事案であって、鉛の作用を疑わしめる末梢神経障害、腹部の疝痛等の症状が認められるか、又は血液検査の結果貧血が認められるものであること。 |
|||||||||||||||||||||||||||||||||||||
| 上に戻る | |||||||||||||||||||||||||||||||||||||